中國疫苗行業研究系列II – 疫苗研發者努力衝線
在本系列上一期「疫苗的過去、現時及未來」中,我們討論了不同類型的疫苗。這一期,我們將討論不同類型的2019新型冠狀病毒疫苗、正研發疫苗的公司以及開發時間表的現狀。
大體而言,現時正在研發的2019新型冠狀病毒病疫苗有兩類:
- 傳統疫苗 – 如重組蛋白疫苗、不活化/減毒活病毒疫苗、及包含病毒蛋白或病毒樣顆粒的腺病毒載體疫苗。這些疫苗構成現有疫苗行業及(由賽諾菲、葛蘭素史克、默克、輝瑞及強生製造的)所有獲批准疫苗的基礎。
- 新型疫苗 – 如僅由病毒遺傳物質組成的mRNA、DNA疫苗,代表項目有Moderna(率先進入臨床試驗階段)、賽諾菲/TranslateBio或輝瑞/BioNtech的疫苗。疫苗一旦注入人體,體內的細胞就會製造病毒抗原引發免疫反應。
傳統疫苗 – 更容易、更快速獲得批准
傳統疫苗的優勢在於,由於對現有成熟技術及製造工序的監管較為寬鬆,因此較易於短時間內獲得監管批准。然而,相較於新型疫苗,將傳統疫苗的產量擴大至數十億劑以滿足潛在需求可能更為困難,或需要更長的時間。根據賽諾菲管理層所透露,該公司利用傳統重組DNA(編碼2019新型冠狀病毒刺突蛋白)技術,在嚴重急性呼吸道系統綜合症(SARS)疫苗的基礎上研發了一種疫苗。更重要的是,該疫苗將於12至18個月後獲得批准,產能將達1至6億劑。賽諾菲還將利用其生產年度Flublok流感疫苗時所使用的基於細胞的製造技術。我們認為,在該公司隨後與葛蘭素史克合作並採用其佐劑後,賽諾菲將偏向保守。同樣地,強生宣佈,其首批腺病毒載體疫苗預計可於2021年初投入緊急用途,研發進度遠超典型疫苗。強生還計畫擴大產能,力求供應十億劑疫苗。
新型疫苗 – 未經檢驗、相較於傳統疫苗,研發速度更快、更易擴大生產規模
在幾周內實現利用病毒基因組測序技術以生產候選疫苗用於測試,Moderna及輝瑞/BioNtech已經達到了這一研發速度。這使得mRNA疫苗研發公司能夠更早進入臨床試驗階段(傳統疫苗預計於2020下半年進入此階段)。可大規模製造的核酸比傳統疫苗所需的蛋白質更有可能實現快速、輕鬆/經濟地擴大生產規模。然而,新型RNA/DNA疫苗的效果並未經過驗證,風險較高、難以把握、且獲得批准的速度可能較慢。
全球約有160個冠狀病毒疫苗項目,其中23個處於臨床試驗階段。
根據世界衛生組織的數據,有160個針對冠狀病毒的活性疫苗項目,其中23個及約140個分別處於臨床試驗階段及臨床前階段。
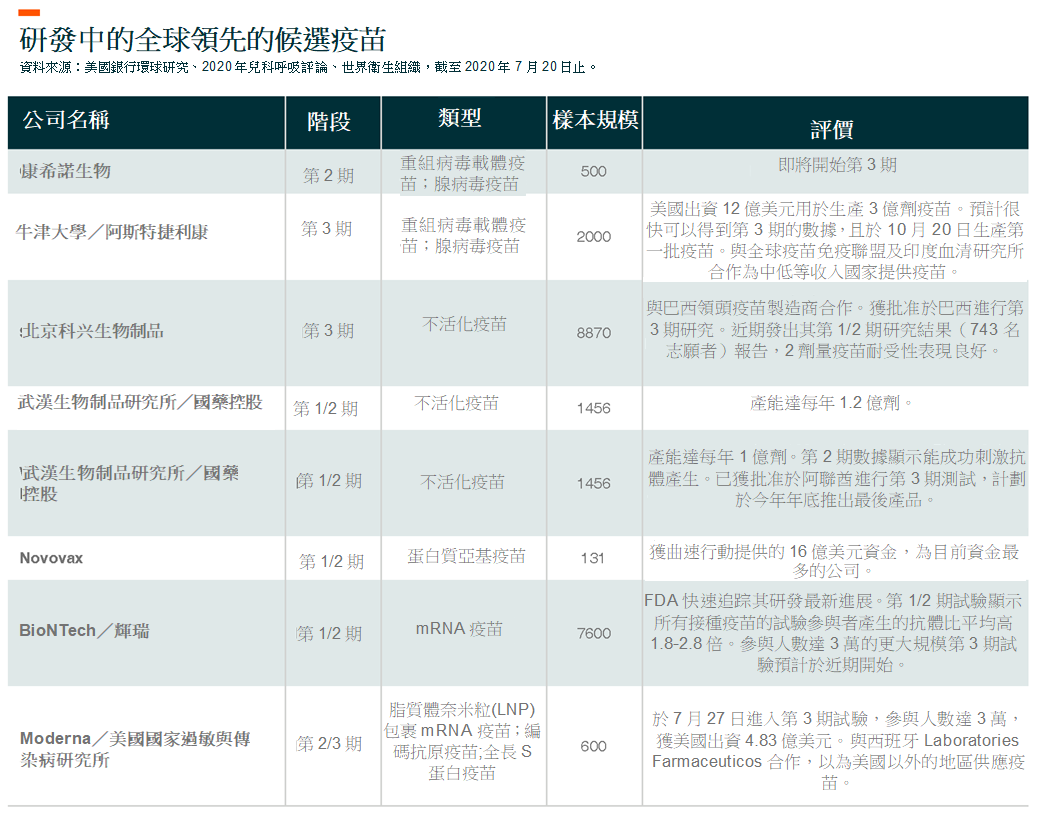
我們將討論具體幾家領先企業的疫苗最新進展。
Moderna – mRNA疫苗領域的領頭羊
Moderna於新英格蘭科學雜誌(NEJM)發表了2019新型冠狀病毒疫苗mRNA-1273的第一期臨床結果(受試患者為45名)。證實了疫苗有正面療效、且較為安全。據近期報導,輝瑞/BNTX疫苗試驗的中核抗體較恢復期血清高出2-3倍,備受推崇,而Moderna的數據高出2-4倍,至少與前兩家一樣優秀。其他的詳細數據亦很重要且均為正面數據,如T細胞反應的激活,這對抵抗感染及增加疫苗的耐久性十分重要。預計第3期試驗(將有3萬參與者)的計劃將很快啟動。Moderna已從美國政府獲得4.83億美元,作為資金以加快疫苗的研發。
康希諾 — 1期數據振奮人心,3期試驗即將開啟
康希諾的候選疫苗Ad5-nCoV:其中國PHI結果顯示出免疫原性的初步跡象,安全可控。在免疫原性方面,大部分受試者注入Ad5-nCoV很快便能引起體液及T細胞免疫反應。50-75%的受試者體內的中和抗體(NAb)增加了4倍。該公司計劃將產能擴大至1至2億劑(包括海外合作夥伴)。
加拿大最新消息:加拿大衛生部已經審查了康希諾在中國的臨床前及臨床數據,並批准康希諾在加拿大開始臨床試驗。
mRNA技術合作夥伴:康希諾還與Precision NanoSystems(PNI)成立了一家合資企業(JV),共同研發mRNA脂質體奈米粒(mRNA-LNP)疫苗對抗2019新型冠狀病毒病。該合資公司將利用PNI專有的RNA疫苗平台,包括脂質體奈米粒輸送系統及製造技術,以推進2019新型冠狀病毒mRNA-LNP候選疫苗的研發進程。
印度血清研究所
印度生產全世界60%的疫苗,佔聯合國年度疫苗採購的60%-80%。153個獲世界衛生組織資格預審的疫苗中,107個來自印度。眾多印度公司中,血清研究所、巴拉特生物技術公司、萬能藥業生物技術公司、Cadila Healthcar及Indian Immunological是疫苗領域的龍頭。
按產量(每年15億劑)計算,血清研究所是全球最大的疫苗製造商、生產的疫苗在逾170個國家銷售。血清研究所與牛津大學(且現時已授權予阿斯特捷利康)就2019新型冠狀病毒疫苗進行合作。該疫苗現時正進行2/3期臨床試驗。血清研究所將負責製造並供應該疫苗。根據於阿斯特捷利康訂立的協議,血清研究所將向中低等收入國家提供10億劑疫苗,其中4億劑將於2020年年底前交付。
相關ETF
Global X中國生物科技ETF 致力於取得與Solactive中國生物科技指數NTR表現密切相關的投資效果、透過投資中國生物技術發展中舉足輕重的公司,從而抓住這一領域的巨大發展潛力。
其他特徵
不受局限的投資方法:透過追蹤新興主題,該基金的組成超越了經典的行業和行業分類。
ETF的投資便利:透過一次買賣交易,該基金可以投資於數十家以中國生物科技為主題的公司。
請點擊此處以了解更多有關Global X中國生物科技ETF 的資料。