中国疫苗行业研究系列II – 疫苗研发者努力冲线
在本系列上一期“疫苗的过去、现时及未来”中,我们讨论了不同类型的疫苗。这一期,我们将讨论不同类型的2019新型冠状病毒疫苗、正研发疫苗的公司以及开发时间表的现状。
大体而言,现时正在研发的2019新型冠状病毒病疫苗有两类:
- 传统疫苗 – 如重组蛋白疫苗、不活化/减毒活病毒疫苗、及包含病毒蛋白或病毒样颗粒的腺病毒载体疫苗。这些疫苗构成现有疫苗行业及(由赛诺菲、葛兰素史克、默克、辉瑞及强生制造的)所有获批准疫苗的基础。
- 新型疫苗 – 如仅由病毒遗传物质组成的mRNA、DNA疫苗,代表项目有Moderna(率先进入临床试验阶段)、赛诺菲/TranslateBio或辉瑞/BioNtech的疫苗。疫苗一旦注入人体,体内的细胞就会制造病毒抗原引发免疫反应。
传统疫苗 – 更容易、更快速获得批准
传统疫苗的优势在于,由于对现有成熟技术及制造工序的监管较为宽松,因此较易于短时间内获得监管批准。然而,相较于新型疫苗,将传统疫苗的产量扩大至数十亿剂以满足潜在需求可能更为困难,或需要更长的时间。根据赛诺菲管理层所透露,该公司利用传统重组DNA(编码2019新型冠状病毒刺突蛋白)技术,在严重急性呼吸道系统综合症(SARS)疫苗的基础上研发了一种疫苗。更重要的是,该疫苗将于12至18个月后获得批准,产能将达1至6亿剂。赛诺菲还将利用其生产年度Flublok流感疫苗时所使用的基于细胞的制造技术。我们认为,在该公司随后与葛兰素史克合作并采用其佐剂后,赛诺菲将偏向保守。同样地,强生宣布,其首批腺病毒载体疫苗预计可于2021年初投入紧急用途,研发进度远超典型疫苗。强生还计画扩大产能,力求供应十亿剂疫苗。
新型疫苗 – 未经检验、相较于传统疫苗,研发速度更快、更易扩大生产规模
在几周内实现利用病毒基因组测序技术以生产候选疫苗用于测试,Moderna及辉瑞/BioNtech已经达到了这一研发速度。这使得mRNA疫苗研发公司能够更早进入临床试验阶段(传统疫苗预计于2020下半年进入此阶段)。可大规模制造的核酸比传统疫苗所需的蛋白质更有可能实现快速、轻松/经济地扩大生产规模。然而,新型RNA/DNA疫苗的效果并未经过验证,风险较高、难以把握、且获得批准的速度可能较慢。
全球约有160个冠状病毒疫苗项目,其中23个处于临床试验阶段。
根据世界卫生组织的数据,有160个针对冠状病毒的活性疫苗项目,其中23个及约140个分别处于临床试验阶段及临床前阶段。
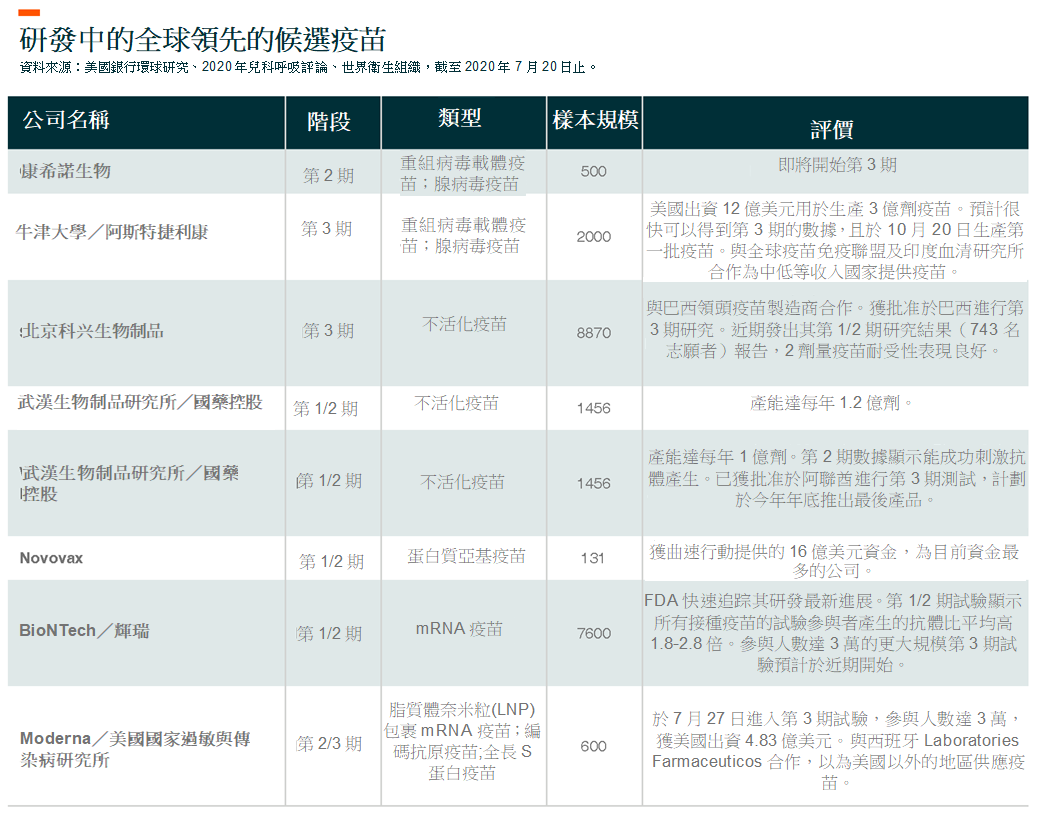
我们将讨论具体几家领先企业的疫苗最新进展。
Moderna – mRNA疫苗领域的领头羊
Moderna于新英格兰科学杂志(NEJM)发表了2019新型冠状病毒疫苗mRNA-1273的第一期临床结果(受试患者为45名)。证实了疫苗有正面疗效、且较为安全。据近期报导,辉瑞/BNTX疫苗试验的中核抗体较恢复期血清高出2-3倍,备受推崇,而Moderna的数据高出2-4倍,至少与前两家一样优秀。其他的详细数据亦很重要且均为正面数据,如T细胞反应的激活,这对抵抗感染及增加疫苗的耐久性十分重要。预计第3期试验(将有3万参与者)的计划将很快启动。Moderna已从美国政府获得4.83亿美元,作为资金以加快疫苗的研发。
康希诺 — 1期数据振奋人心,3期试验即将开启
康希诺的候选疫苗Ad5-nCoV:其中国PHI结果显示出免疫原性的初步迹象,安全可控。在免疫原性方面,大部分受试者注入Ad5-nCoV很快便能引起体液及T细胞免疫反应。50-75%的受试者体内的中和抗体(NAb)增加了4倍。该公司计划将产能扩大至1至2亿剂(包括海外合作伙伴)。
加拿大最新消息:加拿大卫生部已经审查了康希诺在中国的临床前及临床数据,并批准康希诺在加拿大开始临床试验。
mRNA技术合作伙伴:康希诺还与Precision NanoSystems(PNI)成立了一家合资企业(JV),共同研发mRNA脂质体奈米粒(mRNA-LNP)疫苗对抗2019新型冠状病毒病。该合资公司将利用PNI专有的RNA疫苗平台,包括脂质体奈米粒输送系统及制造技术,以推进2019新型冠状病毒mRNA-LNP候选疫苗的研发进程。
印度血清研究所
印度生产全世界60%的疫苗,占联合国年度疫苗采购的60%-80%。153个获世界卫生组织资格预审的疫苗中,107个来自印度。众多印度公司中,血清研究所、巴拉特生物技术公司、万能药业生物技术公司、Cadila Healthcar及Indian Immunological是疫苗领域的龙头。
按产量(每年15亿剂)计算,血清研究所是全球最大的疫苗制造商、生产的疫苗在逾170个国家销售。血清研究所与牛津大学(且现时已授权予阿斯特捷利康)就2019新型冠状病毒疫苗进行合作。该疫苗现时正进行2/3期临床试验。血清研究所将负责制造并供应该疫苗。根据于阿斯特捷利康订立的协议,血清研究所将向中低等收入国家提供10亿剂疫苗,其中4亿剂将于2020年年底前交付。
相关ETF
Global X中国生物科技ETF 致力于取得与Solactive中国生物科技指数NTR表现密切相关的投资效果、透过投资中国生物技术发展中举足轻重的公司,从而抓住这一领域的巨大发展潜力。
其他特征
不受局限的投资方法:透过追踪新兴主题,该基金的组成超越了经典的行业和行业分类。
ETF的投资便利:透过一次买卖交易,该基金可以投资于数十家以中国生物科技为主题的公司。
请点击此处以了解更多有关Global X中国生物科技ETF 的资料。