中国疫苗行业研究系列I – 疫苗的过去、现时及未来
世界上最古老的生物技术药物
疫苗或是世界上古老的生物药物。1796年,一位英国医生利用牛痘脓包中的物质成功为患者接种天花疫苗(天花由天花病毒引起)。至1900年,人类已经研制出天花疫苗及狂犬病疫苗两种病毒疫苗、以及鼠疫疫苗、伤寒疫苗及霍乱疫苗三种细菌疫苗。
免疫接种(或疫苗接种)或许是最具成本效益的公共卫生干预措施,据说每年可预防200万至300万例死亡。
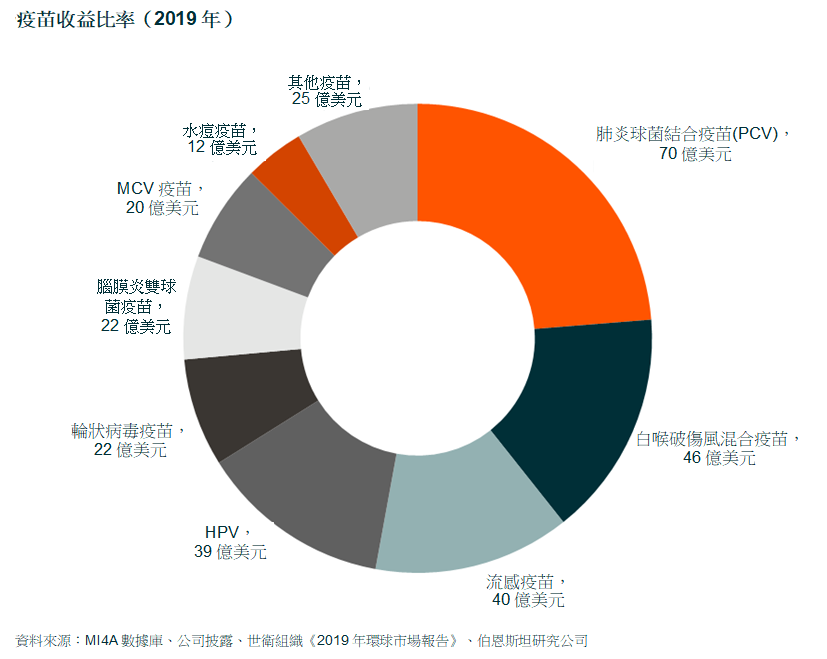
2020年,疫苗市场规模达约350亿美元(2000年约为50亿美元),并以约9%复合年增长率的增速持续增长。过去二十年间,市场规模增长的主要推动因素其一为关键疫苗的推出,包括5价疫苗DTP-HepB-Hib(2004年)、脑膜炎双球菌疫苗(2005年)、儿童肺炎球菌疫苗(HPV)(2000年)、人类乳头瘤病毒疫苗(2006年)及轮状病毒疫苗(2006年),其二为疫苗的普及率增加。
疫苗及其漫长生产流程
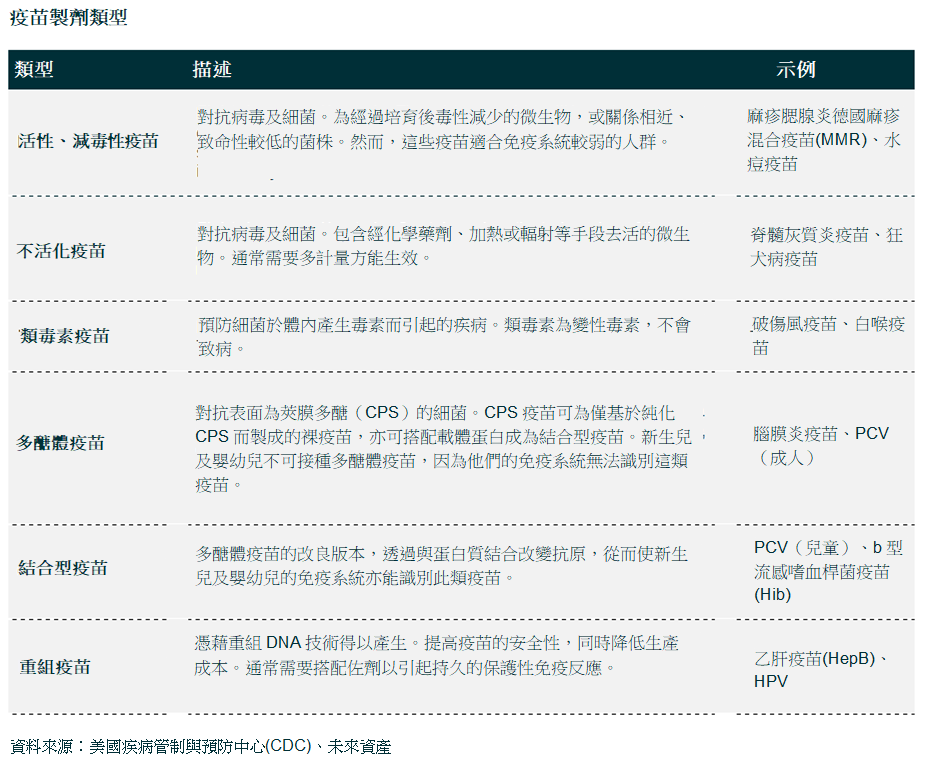
疫苗是一种生物制剂,使受体能对一种特定疾病产生免疫力。疫苗是由基于致病微生物(弱化/失能形式的病原体,或毒素/表面蛋白纯化形式的病原体)的制剂制成。疫苗刺激人体的主要免疫反应,从而产生抗体。
疫苗是复杂的生物产品,可以说是经过一套复杂流程才能得出的产物。其中包括抗原,一种大而复杂的分子,于天然可变的生物过程中产生,因此很难表征抗原。这一可变性意味著生产质素稳定的疫苗需要精湛的制作工艺及测试技术。对专业技术及有关成本的需求为潜在的新参与者设立了较高的行业门槛,即使在非专利疫苗领域亦是如此。
疫苗的生产需要很长的前置时间(8至36个月),生产过程中的每一个步骤及变量都要标准化,且必须受到管控、验证及测试。不同的疫苗成分可能于多个不同的产地生产,并需要进行数百次质素控制测试。对高度无菌及温控环境(标准冷藏链为2-8°C)的要求进一步提高了生产的复杂性。以美国为例,美国食品药品监督管理局规定,新疫苗工厂须至少营运两年后方可向市场投放产品,以证明工厂具备无菌、无外来微粒物质的环境、以及具备疫苗重组及提升疫苗稳定性所需的冻干工艺。这不仅提高了行业准入门槛(由于要求大量启动资金及较高专业技术),还提高了疫苗价格。
寡头型市场
尽管疫苗市场十分具吸引力,但全球疫苗市场的新加入者十分有限。我们认为原因如下:
- 疫苗开发的前置时间很长。
- 制作流程复杂。美国食品药品监督管理局(FDA)、欧洲药品管理局(EMA)、世界卫生组织、各国家监管机构通常每年对疫苗设施进行20至25次实地检查,同时质量保证团队亦进行内部审查。
- 复杂且(与常规药物)不同的分销渠道
- 复杂的法规。以美国为例,美国食品药品监督管理局规定,新疫苗工厂须至少营运两年后方可向市场投放产品,以证明工厂具备无菌、无外来微粒物质的环境、以及具备疫苗重组及提升疫苗稳定性所需的冻干工艺。
按价值计算,前四大公司贡献了全球疫苗市场逾80%的份额。且60%的收入来自于四大疾病。而就销量而言,跨国公司约占总销量的30%,因为领先的公司更注重销售较新一代的、创新型药物,而规模较小的国内公司关注老一代、创新程度较低的疫苗产品,并且仅专心耕耘本土市场。
mRNA技术的广阔前景
mRNA是一种单链分子,它将遗传密码从细胞核中的DNA传递至核糖体(细胞内合成蛋白质的场所)。mRNA药物简单来说是向体内细胞发出的一组指令,刺激特定蛋白质的合成从而帮助预防或对抗疾病。很多公司已研发出或正努力研发技术及方法,从而生产能被细胞识别为体内合成的mRNA序列。
数家跨国公司与开发疫苗领域mRNA技术的公司订立了合作关系。例如,辉瑞与BioNTech合作研发流感候选疫苗、默克在呼吸道合胞病毒领域与Moderna展开合作、同时赛诺菲亦与Translate Bio建立起合作关系。CureVac,与宝灵家殷格翰及礼来共同开发肿瘤产品,并与Genmab合作研发抗体。
Global X中国生物科技ETF,为您带来机遇,可投资数十家深植于中国生物技术领域之公司的机遇,以及把握中国疫苗行业发展的机遇。